細(xì)菌懸液中活菌濃度的檢測(cè)方法:平板點(diǎn)樣技術(shù)VS傳統(tǒng)平板涂布法
[摘要]目的比較平板點(diǎn)樣法與傳統(tǒng)平板涂布計(jì)數(shù)法,建立更為簡(jiǎn)便的細(xì)菌懸液中活菌濃度的檢測(cè)方法。方法將3株A群溶血性鏈球菌制備成多份菌懸液,稀釋成不同梯度,用調(diào)理吞噬實(shí)驗(yàn)中的平板點(diǎn)樣技術(shù)和傳統(tǒng)平板涂布法同時(shí)檢測(cè),比較兩種方法計(jì)數(shù)結(jié)果,分析相關(guān)性和顯著差異。結(jié)果不同菌株和稀釋方法中平板點(diǎn)樣法的結(jié)果均隨菌液稀釋梯度呈現(xiàn)出較好的梯度;兩種方法計(jì)數(shù)結(jié)果呈高度相關(guān)(r=0.84);二者的t檢驗(yàn)結(jié)果比較差異無統(tǒng)計(jì)學(xué)意義(P>0.05)。結(jié)論相對(duì)平板涂布法,平板點(diǎn)樣法計(jì)數(shù)更客觀準(zhǔn)確,檢測(cè)范圍更寬,操作更便捷,適用于菌液濃度的確定。
在臨床細(xì)菌診斷試劑盒的評(píng)價(jià)過程中,菌液濃度的確定是參考品制備的關(guān)鍵步驟,因此菌液濃度的測(cè)定方法應(yīng)當(dāng)準(zhǔn)確、便捷。目前,菌液濃度的測(cè)定和參考品的制備常用濁度法(包括比濁法、分光光度法等)和平皿計(jì)數(shù)法,但濁度法難以區(qū)分活菌與死菌,以及與微生物大小類似的雜質(zhì)。傳統(tǒng)用于測(cè)定菌液內(nèi)活菌量的方法主要是平板涂布法。此方法雖結(jié)果較為準(zhǔn)確,但可計(jì)數(shù)濃度范圍窄,且人眼計(jì)數(shù)不夠客觀;操作復(fù)雜,所需時(shí)間較長(zhǎng),當(dāng)制備大批量參考品時(shí),其計(jì)數(shù)工作量也變得不可忽視,更易因疲勞而使誤差變大。
平板點(diǎn)樣計(jì)數(shù)法是調(diào)理吞噬實(shí)驗(yàn)(opsonophagocytic assay,OPA)中的細(xì)菌濃度檢測(cè)方法。調(diào)理吞噬實(shí)驗(yàn)是評(píng)估肺炎球菌疫苗效價(jià)的實(shí)驗(yàn)方法,其原理是用肺炎球菌疫苗免疫后的血清樣本(抗體)、HL-60細(xì)胞和補(bǔ)體構(gòu)建體外型別特異性抗體介導(dǎo)的調(diào)理吞噬模型,對(duì)一定濃度的肺炎鏈球菌進(jìn)行清除,之后通過檢測(cè)體系中存活肺炎鏈球菌的濃度計(jì)算出血清樣本中的功能抗體活力,實(shí)現(xiàn)對(duì)肺炎球菌疫苗保護(hù)效力的準(zhǔn)確評(píng)估。近年來,美國阿拉巴馬大學(xué)通過長(zhǎng)期探索,建立了優(yōu)化的多重調(diào)理吞噬實(shí)驗(yàn)(multiplexed opsonophagocytic killing assay,MOPA),可同時(shí)對(duì)4種血清型的肺炎球菌功能抗體進(jìn)行檢測(cè),簡(jiǎn)化了實(shí)驗(yàn)流程,減少了工作量并節(jié)約血清樣本,更使得OPA技術(shù)的檢測(cè)通量成倍提高。此實(shí)驗(yàn)方法準(zhǔn)確高效,被WHO推薦用于肺炎球菌疫苗的功能性抗體檢測(cè),且國外部分藥企已經(jīng)開始采用。其中檢測(cè)存活肺炎球菌濃度所用的平板點(diǎn)樣方法是該實(shí)驗(yàn)實(shí)現(xiàn)高效便捷的關(guān)鍵步驟。
在目前申報(bào)檢驗(yàn)的臨床細(xì)菌診斷試劑盒中,A群鏈球菌抗原檢測(cè)試劑盒申報(bào)較多、應(yīng)用較廣,且A群鏈球菌與肺炎球菌寄生部位接近,培養(yǎng)條件較相似。因此本實(shí)驗(yàn)選用A群鏈球菌抗原檢測(cè)試劑盒的國家參考菌株制備懸液,參考調(diào)理吞噬實(shí)驗(yàn)中平板點(diǎn)樣的方法,同時(shí)與傳統(tǒng)平板涂布法比較驗(yàn)證,建立一種更快速簡(jiǎn)便的活菌濃度檢測(cè)法。
1材料與方法
1.1一般材料
菌株是由中國醫(yī)學(xué)微生物菌種保藏管理中心提供A群溶血性鏈球菌CMCC32300、CMCC32301、CMCC32067。試劑是注射用生理鹽水;MH培養(yǎng)基(Bacto)、羊血(陸橋公司);Todd-Hewitt Broth(Bacto)、酵母提取物(Bacto)、瓊脂(Bacto)、2,3,5-氯化三苯基四氮唑TTC(Amresco)、水。培養(yǎng)基為10%羊血培養(yǎng)基:MH培養(yǎng)基10.5 g;水500 mL;在使用前融化培養(yǎng)基,溫度冷卻至50~60℃時(shí)加入羊血50 mL混勻。THYA培養(yǎng)基:Todd-Hewitt Broth培養(yǎng)基12 g;酵母提取物2 g;瓊脂6 g;水500 mL。上層培養(yǎng)基:Todd-Hewitt Broth培養(yǎng)基24 g;酵母提取物4 g;瓊脂6 g;水800 mL。TTC儲(chǔ)液:TTC 1.25 g;水50 mL,用0.22μm濾膜過濾除菌后,于4℃保存。溶液呈淡黃色;若顏色變紅,廢棄,重新制備。
1.2儀器
電子天平(ME204)購自瑞士METTLER TOLEDO儀器(上海)有限公司;恒溫培養(yǎng)箱(LRH-250-Ⅱ)購自廣東省醫(yī)療器械廠;恒溫水浴鍋(XMTD-6000)購自北京市長(zhǎng)風(fēng)儀器儀表公司;超凈工作臺(tái)(SG-603TX)購自BAKER公司;立體菌落計(jì)數(shù)儀購自丹麥Biosense公司;顯微鏡(BX51)購自日本OLYMPUS公司;振蕩器(QL-901)購自海門市其林貝爾儀器制造有限公司。
1.3樣品制備
1.3.1菌懸液制備將A群溶血性鏈球菌CMCC32067、CMCC32300、CMCC32301凍干粉復(fù)蘇后,制成懸液涂布在羊血培養(yǎng)基平板上,在37℃過夜培養(yǎng)。將平板上的菌體刮至10 mL注射用生理鹽水中,制成均一菌懸液。
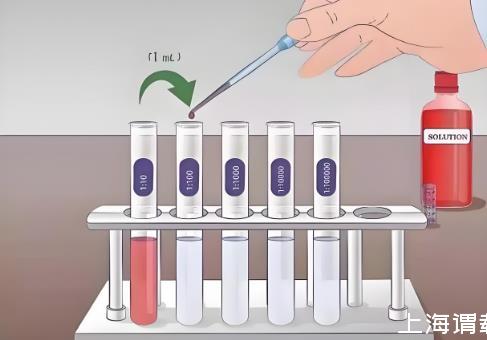
1.3.2梯度稀釋將CMCC32067制備7份菌懸液,將其中5份進(jìn)行1/10系列稀釋8個(gè)梯度,另外2份做1/2系列稀釋18個(gè)梯度;將CMCC32300和CMCC32301各制備1份菌懸液,并進(jìn)行1/10系列稀釋8個(gè)梯度。
1.4平板點(diǎn)樣
1.4.1培養(yǎng)基準(zhǔn)備將THYA培養(yǎng)基融化后,倒于13 cm×13 cm方形培養(yǎng)皿中,25 mL/板;凝固后在超凈臺(tái)內(nèi)開蓋吹30~45 min,備用。將上層培養(yǎng)基融化后保存于50℃水浴中1~2 h,確保溫度至50℃,備用。
1.4.2平板點(diǎn)樣1/10梯度稀釋每個(gè)濃度菌液以及1/2梯度稀釋的后8個(gè)濃度的菌液,分別取10μL滴在THYA方形培養(yǎng)皿左側(cè),每點(diǎn)完一個(gè)樣品立即傾斜平板,使菌液滴流成2~3 cm長(zhǎng),每個(gè)梯度做兩個(gè)平行。待所有樣品點(diǎn)完后,室溫放置20~30 min,讓菌液吸收到瓊脂板上。從水浴中取出上層培養(yǎng)基,取25 mL入25μL TTC儲(chǔ)液混勻,從板子邊緣緩慢傾倒在點(diǎn)樣的THYA平板上。待上層培養(yǎng)凝固,倒置于37℃孵箱中培養(yǎng)過夜,
1.4.3菌落計(jì)數(shù)用菌落計(jì)數(shù)儀統(tǒng)計(jì)每個(gè)點(diǎn)樣條的菌落數(shù)。
1.5平板涂布
分別取各系列菌液中的部分梯度50μL或100μL菌液均勻涂布于羊血平板,各做兩個(gè)平行,倒置于37℃孵箱中培養(yǎng)過夜,手動(dòng)計(jì)數(shù)。
1.6統(tǒng)計(jì)學(xué)方法
將7份菌懸液的各稀釋梯度用兩種平板計(jì)數(shù)法計(jì)數(shù),再用各個(gè)梯度的計(jì)數(shù)結(jié)果分別折算出初始濃度,采用SPSS 13.0對(duì)兩組結(jié)果進(jìn)行相關(guān)性分析和成對(duì)t檢驗(yàn)。以P<0.05為差異有統(tǒng)計(jì)學(xué)意義。
2、結(jié)果與討論
在本實(shí)驗(yàn)中,用不同菌株、不同稀釋方法且多次重復(fù)試驗(yàn),平板點(diǎn)樣法的結(jié)果均隨菌液稀釋梯度呈現(xiàn)出較好的梯度。比較了平板點(diǎn)樣法與平板涂布法計(jì)數(shù)7份CMCC32067的菌懸液的不同濃度梯度,以及不同的血平板點(diǎn)樣量,結(jié)果均顯示出高度相關(guān)性,且差異無統(tǒng)計(jì)學(xué)意義;用兩種平板計(jì)數(shù)方法計(jì)算另外兩株A群溶血性鏈球菌菌液濃度,同樣具有較好的一致性。比較兩種計(jì)數(shù)方法的操作性和準(zhǔn)確性,發(fā)現(xiàn)平板點(diǎn)樣法點(diǎn)樣區(qū)域小、點(diǎn)樣量少,計(jì)數(shù)簡(jiǎn)便,因而可檢測(cè)的濃度范圍比平板涂布法較寬。
用多個(gè)稀釋度的濃度檢測(cè)結(jié)果計(jì)算初始菌液濃度顯示,測(cè)定結(jié)果隨稀釋度提高略有升高,分析原因可能為:①存在稀釋過程中的操作誤差;②點(diǎn)樣區(qū)域有限,在稀釋度低時(shí)菌液濃度高,菌落密集且大小不均,容易漏計(jì)或合并計(jì)數(shù),造成計(jì)算結(jié)果偏低;高稀釋度時(shí)菌液濃度低,菌體可能未落在點(diǎn)樣區(qū)域,造成平行孔之間CV值較大,濃度計(jì)算不準(zhǔn)確。根據(jù)結(jié)果分析,選擇菌落數(shù)在20~100個(gè)之間的點(diǎn)樣區(qū)計(jì)算菌液濃度的偏差較小,點(diǎn)樣濃度最好在2×104~2×102 cfu/mL,將同一菌液的多個(gè)梯度的計(jì)數(shù)結(jié)果平均,計(jì)算初始菌液濃度更為準(zhǔn)確。
由于平板點(diǎn)樣法所需樣品量少、點(diǎn)樣區(qū)域小,可以在一塊方形培養(yǎng)皿里同時(shí)檢測(cè)多個(gè)稀釋度或多種菌液。若待檢樣品多,還可以將初始菌懸液用移液器在96孔板中梯度稀釋后,再用多道移液器同時(shí)點(diǎn)樣多個(gè)梯度或多種菌液,操作更加便捷。且此方法用儀器自動(dòng)計(jì)數(shù),并且可以根據(jù)情況進(jìn)行手動(dòng)調(diào)整,準(zhǔn)確度和效率更高,減少了傳統(tǒng)平板涂布法的涂布不均和人眼計(jì)數(shù)誤差。
對(duì)于其他細(xì)菌檢測(cè)試劑盒,當(dāng)制備試劑盒評(píng)價(jià)參考品時(shí),如果其抗原菌株不能在THYA培養(yǎng)基上生長(zhǎng),如淋病奈瑟菌等,在測(cè)定參考品濃度時(shí)可篩選出適宜其生長(zhǎng)的且透明度好的培養(yǎng)基點(diǎn)樣,以便于TTC顯色后用儀器計(jì)數(shù),這部分研究將在本室的后續(xù)工作中進(jìn)行。
綜上所述,相較于平板涂布法,用平板點(diǎn)樣法檢測(cè)菌液濃度更加快捷,簡(jiǎn)便,上樣量少,且檢測(cè)結(jié)果更準(zhǔn)確客觀,檢測(cè)范圍寬,平均多個(gè)梯度后計(jì)算更加縮小了誤差,可以用于大批量試劑盒參考品的制備。
相關(guān)新聞推薦
1、基于革蘭氏陽性菌生長(zhǎng)曲線等指標(biāo)評(píng)價(jià)纖維素基抑菌材料L-Met改性MCC(M-MCC)抑菌效果(四)
2、辣木籽提取物制備、對(duì)蠟樣芽孢桿菌的抑制作用及在在液態(tài)乳中的應(yīng)用(一)
3、莠去津?qū)λ靖H土壤微生物菌群結(jié)構(gòu)及降解基因豐度的影響(二)
4、發(fā)根農(nóng)桿菌Ri質(zhì)粒構(gòu)建燈盞花發(fā)根最優(yōu)的培養(yǎng)體系(二)
