327株不同種類鏈球菌的體外藥敏試驗檢測方法(一)
鏈球菌是臨床能夠分離到的常見致病菌之一,尤其是肺炎鏈球菌、化膿鏈球菌、無乳鏈球菌等,對于人類,尤其是兒童的健康存在巨大威脅。隨著目前廣譜抗菌藥物在臨床中的應用日益增多,臨床上鏈球菌對于某些抗菌藥物的耐藥情況也日益嚴重。因此,臨床分離鏈球菌屬的體外藥敏試驗檢測顯得尤為重要。目前,臨床上已經有商業化的鏈球菌藥敏檢測試劑,并且已得到較為普遍的應用,但是不同廠家或不同方法學之間存在較大差異。本文通過考察一種國產商業化鏈球菌藥敏板與微量肉湯稀釋法對327株不同種類鏈球菌的體外藥敏試驗檢測,進而評估該新型商業化鏈球菌藥敏板卡的體外藥敏檢測性能,以期為臨床鏈球菌屬引起的感染性疾病提供更合理的用藥指導。
1 材料與方法
1.1材料
收集2018-2019年來源于鄭州市中心醫院、鄭州市人民醫院、南陽市中心醫院和河南省人民醫院的327株鏈球菌屬臨床菌株,包括肺炎鏈球菌107株,化膿鏈球菌41株,緩癥鏈球菌51株,無乳鏈球菌55株,停乳鏈球菌7株,星座鏈球菌13株,咽頰炎鏈球菌15株,草綠色鏈球菌8株,中間鏈球菌22株,血鏈球菌8株。標準菌株:肺炎鏈球菌(ATCC49619)。
1.2儀器與試劑
上海精科科技公司的酸度計,廈門致微公司的高壓滅菌鍋,瑞士METTLER TOLEDO公司的電子天平,金壇市科析儀器公司的振蕩儀,上海躍進公司的恒溫培養箱,法國生物梅里埃公司的比濁儀,美國SIGMA公司的快速離心機,中國海爾集團的-20 ℃冰箱,美國Thermo公司的移液器,美侖生物科技公司的頭孢曲松、利福平、氨芐西林、頭孢呋辛、美羅培南、青霉素、氯霉素、頭孢噻肟、阿莫西林/克拉維酸、頭孢吡肟、四環素、利奈唑胺、替加環素、左氧氟沙星、克林霉素、莫西沙星、甲氧芐啶、復方磺胺甲噁唑、萬古霉素、紅霉素抗菌藥物標準品,購自Oxoid公司的M-H干粉、脫纖維綿羊血、礦物油,血瓊脂平板(鄭州安圖生物工程股份有限公司),鏈球菌藥敏檢測試劑盒(比色/比濁法,鄭州安圖生物工程股份有限公司),洛陽昊華公司的無水乙醇,國藥集團公司的二甲基亞砜。
1.3方法
使用血瓊脂平板對質控菌株和臨床菌株進行活化,利用0.85%生理鹽水將各臨床菌株制備成0.5麥氏單位的菌懸液,根據美國臨床和實驗室標準協會(CLSI)《需氧菌的稀釋法藥敏試驗方法》關于鏈球菌屬細菌藥敏試驗所用培養基制備的規定,將M-H干粉按照要求的量充分溶解并調節pH值至7.0左右,121 ℃高溫高壓滅菌15 min,滅菌的M-H肉湯冷卻后,添加2.5%~5.0%的脫纖維綿羊血,混勻后備用。分別稱取頭孢噻肟等20種抗菌藥物標準品,根據需要考核試劑的各種抗菌藥物濃度分布及CLSI標準對于肉湯稀釋法操作過程的嚴格規定,使用合適的溶解試劑進行抗菌藥物的溶解并加入96孔板內,每孔加入10 μL的10倍于檢測濃度的抗菌藥物溶解液,并使用大型真空干燥箱進行快速干燥處理,保存備用。
微量肉湯稀釋法操作:取90 μL加血M-H肉湯加入96孔酶標板,將板立即置于Bioscreen C自動微生物生長曲線分析系統上。;每種抗菌藥物進行3次平行試驗,將已制得的0.5麥氏單位質控菌懸液稀釋200倍后,各取10 μL加入酶標板各孔內,滴加1滴礦物油液封并置于35~37 ℃溫箱內培養24 h。待評價鏈球菌藥敏試劑盒操作過程:取出1瓶培養液,向其中添加1滴顯色液和100 μL菌懸液,混勻后向120孔鏈球菌藥敏板每孔加入100 μL菌懸液,滴加礦物油后蓋上蓋子置于35~37 ℃溫箱內培養24 h。兩種操作均要求首先進行肺炎鏈球菌(ATCC49619)的質控,合格后才能進行臨床菌株試驗。依據CLSI文件M100-S29標準,對藥敏試驗結果和敏感性結果進行記錄和統計分析。
1.4統計學處理
對兩種方法所測得的最小抑菌濃度(MIC)結果及菌株敏感性結果按照菌株分類進行統計學分析,采用SPSS23.0統計軟件對數據進行分析處理。計數資料以例數或百分率表示,采用χ2檢驗進行比較。以P<0.05為差異有統計學意義。根據CLSI的M52標準進行菌株敏感性比較分析;統計出3種方法的基本一致性(EA,即不同MIC測定方法在±1個稀釋倍數范圍內的結果一致性)和分類一致性(CA,即不同方法測定的菌株對抗菌藥物敏感性的一致性),另外,對于菌株敏感性,需要進行非常重大誤差(VME,即耐藥誤判為敏感)、重大誤差(ME,即敏感誤判為耐藥)和微小誤差(mE,即中介報告為敏感或耐藥)結果的測定。美國食品藥品監督管理局標準規定指出,CA≥90%、EA≥90%、VME≤1.50%、ME≤3.00%、mE<3.00%為可接受范圍。
2 結 果
2.1考核試劑盒與微量肉湯稀釋法EA測定結果
統計鏈球菌藥敏試劑盒與微量肉湯稀釋法的檢測結果,對其EA進行統計分析,按照CLSI標準對于不同方法學結果差異的規定,不同測定方法的MIC差值≤1個倍比梯度認為是正確測定值。EA檢測結果見表1。新型鏈球菌藥敏板與“金標準”微量肉湯稀釋法共測定327株鏈球菌的體外藥敏檢測,在EA方面,按照測試結果總量統計,新型鏈球菌藥敏板與微量肉湯稀釋結果差異在±1個稀釋倍數內的整體符合結果個數/總結果個數為6 509/6 540,整體EA為99.53%。對于所涵蓋的抗菌藥物種類:頭孢曲松、利福平、頭孢呋辛、青霉素、氯霉素、頭孢噻肟、阿莫西林/克拉維酸、頭孢吡肟、四環素、利奈唑胺、替加環素、左氧氟沙星、克林霉素、莫西沙星、萬古霉素、紅霉素的EA均為100.00%;氨芐西林EA為97.86%;美羅培南EA為96.94%;復方磺胺甲噁唑EA為97.55%;紅霉素/克林霉素誘導試驗EA為98.17%;對于所測臨床菌株,隨機選取10株進行結果重復性測試,檢測結果與已測結果一致。
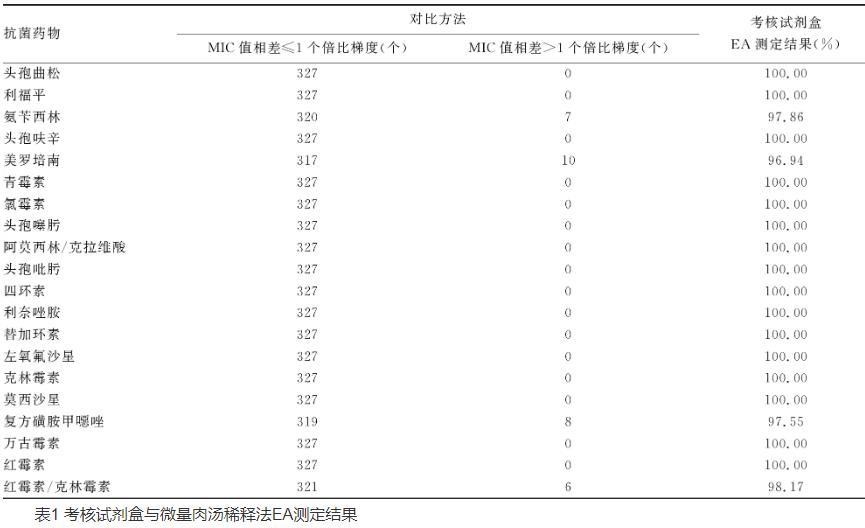
表1 考核試劑盒與微量肉湯稀釋法EA測定結果
2.2考核試劑盒與微量肉湯稀釋法CA測定結果
對兩種測定方法的體外藥敏檢測的CA進行統計,結果表明,新型鏈球菌藥敏板與“金標準”微量肉湯稀釋法測定共進行327株鏈球菌的體外藥敏檢測,兩種方法的整體CA為97.40%,VME為0.09%,ME為0.59%,mE為1.92%。新型鏈球菌藥敏板與“金標準”微量肉湯稀釋法的CA測定結果差異無統計學意義(P>0.05)。見表2。
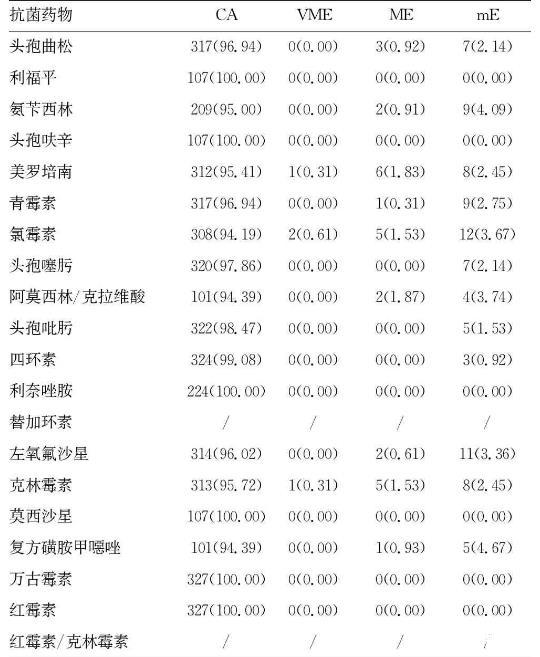
表2 考核試劑盒與微量肉湯稀釋法CA測定結果[n(%)]
相關新聞推薦
1、不同微生物菌劑處理對秸稈降解率、可培養細菌/真菌/放線菌數量影響
